EMMANUELLE CHARPENTIER - 1968'de, Fransa’da, Juvisy-sur-Orge’da doğdu. Paris’teki Pierre ve Marie Curie Üniversitesi’nde biyoloji, mikrobiyoloji ve biyokimya okudu. Doktora derecesini 1995’te, Paris’teki Pasteur Enstitüsü’nden aldı. Halen, Almanya’nın Berlin kentindeki Max Planck Enstitüsü’nün Patojen Bilim Birimi’nin yöneticisidir.

JENNIFER A. DOUDNA - 1964'te ABD’de Washington, D.C’de doğdu. California’daki Pomona Kolejinde biyokimya okudu. Doktorasını 1989’da, ABD’deki Harvard Tıp Fakültesi'nde tamamladı. Halen, ABD’deki California Üniversitesi Berkeley Kampüsü’nde ve Howard Hughes Tıp Enstitüsü’nde araştırmacı olarak çalışmaktadır.
Emmanuelle Charpentier ve Jennifer Doudna, gen teknolojisinin en keskin araçlarından biri olan CRISPR / Cas9 genetik makasını bulmaları nedeniyle 2020 yılı Nobel Kimya Ödülü'ne layık görüldüler. Araştırmacılar bu makası, hayvanların, bitkilerin ve mikroorganizmaların DNA'sını son derece yüksek hassasiyetle değiştirmek için kullanabiliyorlar. Bu teknoloji moleküler yaşam bilimlerinde bir devrim yarattı, bitki ıslahı için yeni fırsatlar getirdi, yenilikçi kanser tedavilerine katkıda bulunuyor ve kalıtsal hastalıkları tedavi etme hayalini gerçekleştirme potansiyeline sahip. - Nobel Kraliyet Akademisi
 Bilimin çekici yanlarından biri de tahmin edilemez oluşudur. Bir düşüncenin veya sorulan bir sorunun hangi yöne ilerleyeceğini öceden bilemezsiniz. Meraklı bir zihnin yolculuğu bazen bir çıkmaz sokakta sonlanır, bazen de içinde gidilmesi yıllar alan dikenli bir labirentte.
Bilimin çekici yanlarından biri de tahmin edilemez oluşudur. Bir düşüncenin veya sorulan bir sorunun hangi yöne ilerleyeceğini öceden bilemezsiniz. Meraklı bir zihnin yolculuğu bazen bir çıkmaz sokakta sonlanır, bazen de içinde gidilmesi yıllar alan dikenli bir labirentte.
Ama, her seferinde olduğu gibi şimdi de, o meraklı zihin, hiç dile getirilmemiş olasılığın ufuklarına bakan ilk kişi olduğunun farkındadır.
CRISPR-Cas9 adlı gen editörü nefes kesici potansiyele sahip beklenmedik bir buluş. Emmanuelle Charpentier ve Jennifer Doudna Streptococcus bakterisinin bağışıklık sistemini araştırmaya başladıklarında, fikirlerinden biri yeni bir antibiyotik formu geliştirebilecekleri yönündeydi. Bunun yerine, genetik materyalde hassas kesiler yaparak hayatın kodunu kolayca değiştirmeyi mümkün kılmakta kullanılabilecek bir moleküler araç icad ettiler.
Herkesi etkileyen güçlü bir araç
Bulunmasından sadece sekiz yıl sonra, bu genetik makas yaşam bilimlerini yeniden şekillendirdi. Şimdi biyokimyacılar ve hücre biyologları artık farklı genlerin işlevlerini ve hastalığın ilerlemesinde oynadıkları olası rolleri kolaylıkla araştırabiliyorlar. Araştırmacılar, bitki ıslahında, bitkilere, daha sıcak bir iklimde kuraklığa dayanma yeteneği gibi özellikler kazandırabiliyorlar, tıpta yeni kanser tedavileri ve kalıtsal hastalıkları iyileştirmeyi hedefleyen öncü çalışmalar yapıyorlarlar.
CRISPR-Cas9'un nasıl kullanılabileceğine dair, aralarında etik olmayanların da bulunduğu, neredeyse sonsuz sayıda örnek var. Tüm güçlü teknolojilerde olduğu gibi, bu genetik makas uygulamalarının da yasal düzenlemelerle denetlenmesi gerekir.
2011'de, ne Emmanuelle Charpentier ne de Jennifer Doudna Porto Riko'da bir kafedeki ilk görüşmelerinin, hayat değiştiren bir karşılaşma olduğunun farkında değillerdi. Başlangıçta işbirliği yapmalarını öneren kişi olan Charpentier'i anlatarak başlayacağız.
Charpentier patojenik bakterilerden etkileniyor
Bazı insanlar onu azimli, özenli ve titiz olarak adlandırmaktaydı. Diğerleri Emmanuelle Charpentier'in her zaman beklenmeyenin arayışında olduğunu söylüyor. Kendisi, Louis Pasteur'den alıntı yapıyor: "Şans, hazırlıklı olan zihinleri tercih eder”. Yeni keşifler yapma dürtüsü ile özgür ve bağımsız olma arzusu onun yolunu belirliyor. Doktora çalışmalarını yaptığı Paris'teki Institut Pasteur de dahil olmak üzere, beş farklı ülkenin yedi farklı şehrindeki on farklı kurumda yaşadı.
Çevresi ve yaklaşımları değişti, ancak araştırmalarının çoğunun hep ortak bir paydası oldu: patojenik bakteriler. Neden bu kadar agresifler? Antibiyotiklere karşı dirençlerini nasıl geliştiriyorlar Ve ilerlemelerini durdurabilecek yeni tedaviler bulmak mümkün mü?
Emmanuelle Charpentier, 2002 yılında Viyana Üniversitesi'nde kendi araştırma grubunu kurduğunda, insanlığa en büyük zararı veren bakterilerden biri olan Streptococcus pyogenes'e odaklandı. Bu bakteri her yıl milyonlarca insana bulaşır ve genellikle bademcik iltihabı, iltihaplı isilik gibi kolayca tedavi edilebilir enfeksiyonlara neden olur. Bununla birlikte, yaşamı tehdit eden sepsise de neden olabilir ve gövdedeki yumuşak dokuları parçalayabilir. Bu yüzden “et yiyici” olarak da bilinir.
S. pyogenes'i daha iyi anlamak için Charpentier, bu bakterinin genlerinin nasıl düzenlenmiş olduğunu ayrıntılı biçimde araştırarak işe başladı. Bu kararı, genetik makasın keşfine giden yoldaki ilk adım oldu. Ama bu yolda daha fazla ilerlemeden önce, Jennifer Doudna hakkında da daha fazla bilgi sahibi olmalıyız. Çünkü, Charpentier, S. pyogenes üzerinde ayrıntılı araştırmalar yaparken, Doudna henüz CRISPR olarak anılan kısaltmasıyı yeni duyuyordu.
Bilim - bir dedektif hikayesindeki kadar macera
Çocukluğu Hawaii'de geçen Jennifer Doudna, çocukken bile öğrenme yönünde güçlü bir dürtüye sahipti. Bir gün, babası James Watson'ın The Double Helix (: İkili Sarmal) adlı kitabını yatağına koydu. James Watson ve Francis Crick'in DNA molekülünün yapısını nasıl çözdüğünü anlatan, dedektif hikayesi tarzındaki bu öykü, okul kitaplarında okudularına hiç benzemiyordu. Bilimsel süreç Jennifer’i büyüledi ve bilimin, bulgulardan daha fazla birşey olduğunu fark etti.
Ancak, bilimsel gizemleri çözmeye başladığında, dikkati DNA'da değil, moleküler kardeşi RNA üzerindeydi. 2006 yılında - onunla tanıştığımızda – California Üniversitesi’nin Berkeley kampüsünde bir araştırma grubuna liderlik ediyordu ve RNA üzerinde yirmi yıllık çalışma deneyimine sahipti. Çığır açıcı projeleri koklayabilen başarılı bir bilim insanı olarak ünlenmişti ve kısa bir süredir RNA müdahalesi (RNA interference) olarak bilinen heyecan verici yeni bir alana girmişti.
Uzun yıllar boyunca araştırmacılar, RNA'nın temel işlevini anladıklarına inanıyorlardı, ancak aniden hücrelerdeki gen faaliyetini düzenlemeye yardımcı olan çok sayıda küçük RNA molekülü keşfettiler. Jennifer Doudna’nın RNA müdahalesine katılmasına, 2006’da farklı bir bölümdeki bir meslektaşından aldığı telefondan neden oldu.
Bakteriler eski bir bağışıklık sistemi taşırlar
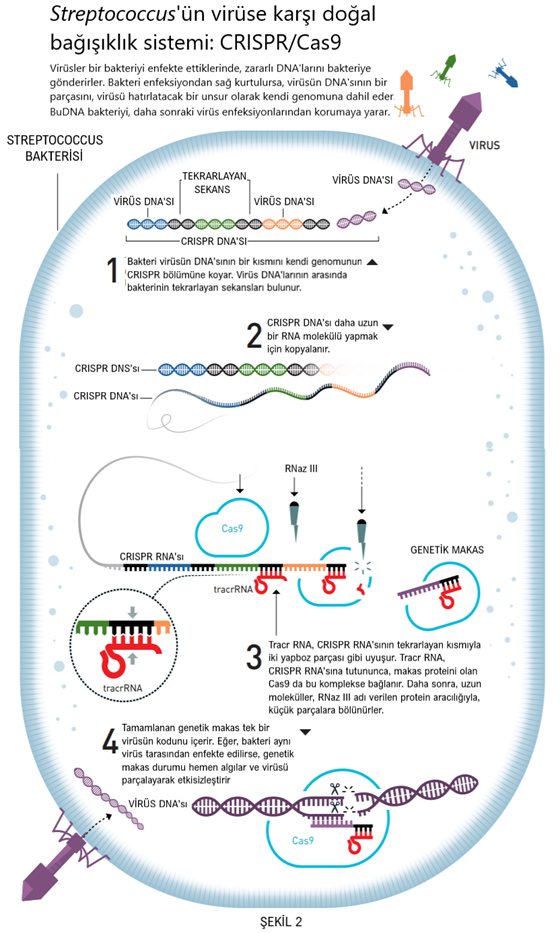
Mikrobiyolog olan meslektaşı, Doudna'ya yeni bir keşiften bahseder: son derece farklı bakterilerin genetik materyali ile archaea adlı bir mikroorganizmayı birlikte incelediklerinde, tekrarlayan DNA dizilerinin şaşırtıcı derecede iyi korunmuş halde bulunduğunu buldular. Aynı kod, kendine özgü dizilime sahip olan farklı sekansların arasında kalan kesimlerde defalarca tekrar tekrar görünür (şekil 2). Yani, bir kitabın birbirine benzemeyen cümlelerinin arasında hep aynı kelimenin tekrarlanması gibi bir durum söz konusudur.
Bu tekrarlayan sekans dizilerine düzenli aralıklarla kümelenmiş kısa palindromik tekrarlar (Clustered Regularly Interspaced Short Palindromic Repeats) denir. CRISPR olarak kısaltılır. İlginç olan, CRISPR’daki benzersiz ve tekrarlanmayan sekansların çeşitli virüslerin genetik kodlarıyla eşleşiyor olmasıdır. Bu nedenle şu anki düşünce, bu tekrarlanmayan sekansların, bakterileri ve arkeayı virüslerden koruyan eski bir bağışıklık sisteminin bir parçası olduğu yönündedir. Hipoteze göre, bakteri, bir virüs enfeksiyonundan kurtulmayı başarırsa, virüsün genetik kodunun bir kısmını, enfeksiyonu hatırlatmak üzere kendi genomuna ekler.
Meslektaşı, tüm bunların nasıl çalıştığını henüz kimsenin bilmediğini belirtir, ancak, bakteriler tarafından virüsü nötralize etmek için kullanılanlan mekanizmanın, Doudna’nın çalıştığı RNA interferansına benzediğinden kuşkulanılmaktadır.
Doudna karmaşık mekanizmanın bir makinenin ilişki haritasını çıkarır
Bu haber hem dikkat çekici hem de heyecan vericidir. Bakteriler eski bir bağışıklık sistemine sahip iseler, o zaman iş büyümektedir. bu büyük bir anlaşma. Jennifer Doudna’nın moleküler karmaşıklık hakkındaki sezgisin hayat buluyor demektir ve CRISPR sistemi hakkında öğrenebileceği her şeyi öğrenmeye başlar.
Araştırmacıların CRISPR dizilerine ek olarak , CRISPR ile ilişkili (CRISPR-associated ya da kısaltılmış haliyle cas olarak anılanr) özel genleri keşfettikleri ortaya çıktı. Doudna'nın ilginç bulduğu şey, bu genlerin, DNA’yı çözme ve kesme konusunda özelleşmiş olan ve halen bilinen proteinleri kodlayan genlere çok benziyor olmalarıdır. Bu durumda, Cas proteinleri de aynı işleve mi sahiptirler? Virüsün DNA’sını bölmekte midirler?
Araştırma grubunu çalıştırır ve birkaç yıl sonra, grup birkaç farklı Cas proteininin işlevini ortaya çıkarırlar. Buna paralel olarak, diğer üniversitelerden de bir kaç araştırma grubu
yeni keşfedilen CRISPR / Cas sistemini incemektedir. Onların ortaya koydyğu ilişki haritaları, bakterilerin bağışıklık sistemleri çok farklı biçimler alabildiğini gösterir. Doudna’nın üzerinde çalıştığı CRISPR / Cas sistemi “Sınıf 1”e aittir. Virüsü etkisizleştirmek için pekçok farklı Cas proteinine gerek sinimi olan karmaşık bir mekanizmaya sahiptir. “Sınıf 2” sistemleri, daha az proteine ihtiyaç duydukları için önemli ölçüde daha basittirler. Dünyanın başka bir yerinde ise, Emmanuelle Charpentier böyle bir sistemle henüz karşılaşmaktadır. Şimdi tekrar Charpentier’ye dönelim.
CRISPR sistemi bulmacasının yeni ve bilinmeyen bir parçası
Emmanuelle Charpentier'yi bıraktığımızda Viyana'da yaşıyordu, ancak 2009'da, İsveç'in kuzeyindeki Umeå Üniversitesi'nde, iyi araştırma fırsatları olan bir pozisyona geçti. Dünyanın öylesi ücra bir köşesine taşınma konusuna uyarıldı. Ama uzun ve karanlık kış, iş için ona bol bol huzur ve sessizlik sağlıyordu.
Buna da ihtiyacı vardı. Aynı zamanda küçük, gen düzenleyici RNA molekülleri ile ilgileniyordu ve Berlin'deki araştırmacılarla birlikte çalışarak, S. pyogenes'te bulunan küçük RNA'ların ilişki haritasını çıkardı. Sonuçlar, düşünmesi gereken çok şey Verdi. Çünkü bu bakteride büyük miktarlarda bulunan küçük RNA moleküllerinden biri, henüz bilinmeyen bir varyanttı ve de bu RNA'nın genetik kodu, bakterinin genomundaki tuhaf CRISPR sekansına çok benziyordu.
İkisi arasındaki benzerlikler, Charpentier'in birbirleriyle bağlantılı olduklarından şüphelenmesine neden oldu. Bunların genetic kodlarının dikkatli analizi, küçük ve bilinmeyen RNA molekülünün bir kısmının, CRISPR’ın tekrarlayan kısmıyla uyuştuğunu ortaya çıkardı. Bu, birbirine mükemmel şekilde uyan iki bulmaca parçasını bulmak gibiydi (şekil 2).
Charpentier, CRISPR ile hiç çalışmamıştı, ancak araştırma grubu, S. pyogenes'teki CRISPR sistemini haritalamak için kapsamlı mikrobiyolojik dedektiflik çalışmaları başlatmıştı. Bu sisteme ait sınıf 2'nin, virüsün DNA'sını ayırmak için yalnızca Cas9 adlı Cas proteinine ihtiyacının olduğu zaten biliniyordu. Charpentier, bilinmeyen ama trans-aktifleştirici crispr RNAsı olarak adlandırılan RNA molekülünün (kısaltması: tracrRNA), uzun RNA’lar için gerekli olan belirleyici bir işleve de sahip olduğunu gösterdi.
Yoğun ve hedefe yönelik deneylerin ardından Emmanuelle Charpentier,
tracrRNA’nın keşfiyle ilgili sonuçları 2011’in Mart ayında yayımladı. Çok heyecan verici bir şeyin peşinde gitmekte olduğunun bilincindeydi. olduğunu biliyor. Mikrobiyoloji alanında uzun yıllara dayanan deneyimi vardı ve CRISPR-Cas9 konusunda sürdürdüğü araştırmasında
bir biyokimyacı ile ortak çalışma yapmak istiyordu. Doğal seçim Jennifer Doudna oldu. Ve o bahar, bulguları hakkında bir konuşma yapmak için Porto Riko'daki bir konferansa davet edildi. Amacı, bu yetenekli Berkeley araştırmacısıyla tanışmaktı.
Porto Riko’daki bir kafede hayatları değiştiren bir toplantı
Tesadüfen konferansın ikinci gününde bir kafede buluşurlar. Doudna'nın bir meslektaşı
onları tanıştırır ve ertesi gün Charpentier, Doudna’ya başkentin eski mahallelerini birlikte keşfetmeyi teklif eder. Arnavut kaldırımlı sokaklarda dolaşırken araştırmaları hakkında konuşmaya başlarlar. Charpentier, Doudna'nın bir ortak çalışmaya ilgi duyup duymadığını merak etmektedir. Cas9'un, S. pyogenes'in basit yapılı sınıf 2 sistemindeki işlevini incelemeye katılmak ister miydi?
Konu, Jennifer Doudna'yı çeker ve hem kendileri hem de meslektaşları, dijital ortamda yürüttükleri toplantılarla proje hakkında planlar yaparlar. Merak ettikleri hususlar, CRISPR-RNA'nın, virüsün DNA'sını tanımlamak için gerekli olup olmadığı ve ve Cas9'un DNA molekülünü kesen makas olup olmadığıdır. Ancak, bunu in vitro test ettiklerinde hiçbir şey olmaz. DNA molekülü bozulmadan kalır. Neden? Deney koşullarında bir sorun mu vardır? Yoksa, Cas9'un tamamen farklı bir işlevi var mı?
Çok sayıda beyin fırtınası ve çok sayıda başarısız deneyden sonra, araştırmacılar nihayet
tracrRNA’yı testlerine dahil ederler. Daha önce, tracrRNA'nın, yalnızca CRISPR-RNA aktif formuna bölündüğünde gerekli olduğuna inanıyorlardı (şekil 2), ancak Cas9 tracrRNA'ya eriştiğinde herkesin beklediği şey gerçekleşti: DNA molekülü iki parçaya bölündü.
Evrimsel çözümler çoğu zaman araştırmacıları şaşırtmıştır, ancak bu olağanüstü bir şeydi.
Streptococci'nin virüslerden korunmak için geliştirdiği silah basit ve etkiliydi ama çok parlaktı. Genetik makasın tarihi burada kilitlenmiş olabilirdi. Charpentier ve Doudna, bir bakteride, insanlık için büyük acılara neden olan temel bir mekanizmayı ortaya çıkarmışlardı. Bu keşif son derece şaşırtıcıydı, ancak şans, hazırlıklı zihinleri tercih ediyordu.
Çığır açan bir deney
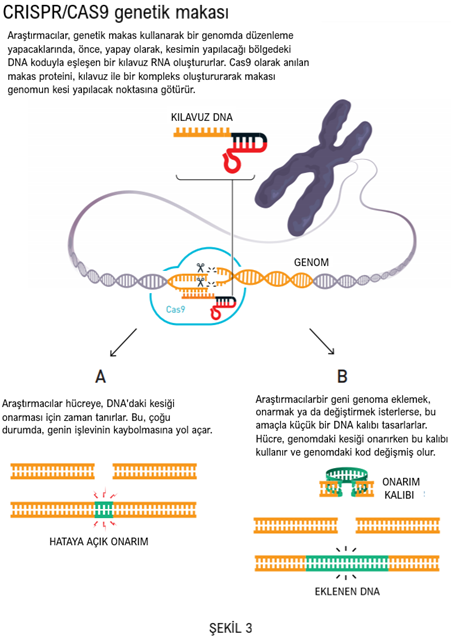
Araştırmacılar, genetik makası basitleştirmeye karar verirler. TracrRNA ve CRISPR-RNA hakkındaki yeni bilgilerini kullanarak, ikisini, kılavuz RNA adını verdikleri tek bir molekülde nasıl birleştireceklerini buldular. Genetik makasın bu basitleştirilmiş varyantıyla, daha sonra çığır açıcı bir deney yaptılar: bu genetik aracı denetleyerek, DNA’yı, kendi belirledikleri bir noktadan kesmesini inceleme altına aldılar.
O ana kadar, araştırmacılar büyük bir ilerlemenin eşiğinde olduklarını biliyorlardı. Doudna'nın laboratuvarındaki dondurucuda bulunan bir geni aldılar ve genin kesilmesini istedikleri beş noktayı belirlediler. Daha sonra makasın CRISPR kısmının kodunu, istedikleri kesimlerin yapılacağı yerlerin koduyla eşleşecek biçimde değiştirdiler (şekil 3). Sonuç müthişti. DNA molekülleri tam olarak doğru yerlerden bölünmüştü.
Genetik makas yaşam bilimlerini değiştiriyor
Emmanuelle Charpentier ve Jennifer Doudna, CRISPR/Cas9 genetik makas buluşlarını 2012’de yayımladıktan kısa bir süre sonra, çeşitli araştırma grupları bu aracın, hem farelerden hem de insanlardan alınan hücrelerde genomu değiştirmekte kullanılabileceğini göstererek müthiş bir gelişmenin önünü açtılar. Önceden, bir hücre, bitki veya organizmadaki genleri değiştirmek ya uzun zaman almaktaydı ya da bazen imkansızdı. Genetik makasın kullanımıyla, araştırmacılar –ilkesek olarak- diledikleri genomda kesimler yapabilirler. Bunun ardından, hücrenin DNA onarımı için doğal sistemlerini kullanmak kolaydır. Böylece yaşamın kodu yeniden yazılmış olur (Şekil 3).
Bu gen aracının kullanımı çok kolay olduğu için artık temel araştırmalarda yaygınlaşmış durumda. Farklı genlerin nasıl işlediğini ve bir hastalığın seyri sırasında nasıl etkileştiklerini anlamak amacıyla hücrelerin ve laboratuvar hayvanlarının DNA'sını değiştirmek için kullanılıyor.
Genetik makas da bitki ıslahında da standart bir araç haline geldi. Araştırmacıların daha önce kullandıkları yöntemlerde, bitki genomlarını değiştirmek için genellikle antibiyotik direnci sağlayacak genlerin eklenmesi gerekiyordu. Mahsuller ekildiğinde ise, bu antibiyotik direncinin çevredeki mikroorganizmalara yayılma riski ortaya çıkıyordu. Genetik makas sayesinde, araştırmacıların, artık genomda çok kesin değişiklikler yapabilmeleri nedeniyle, bu eski yöntemleri kullanmasına gerek kalmadı. Diğer şeylerin yanı sıra, pirincin topraktan ağır metalleri soğurmasını sağlayan genleri düzenleyerek, kadmiyum ve arsenik seviyeleri dshs düşük pirinç türlerin oluşmasını sağladılar. Araştırmacılar, sıcak iklimlerde oluşabilen- kuraklığa daha iyi dayanabilen, böceklere ve diğer zararlılara karşı, böcek öldürücü kullanmadan dayanım sağlayan ürünler de geliştirdiler.
Kalıtsal hastalıkları tedavi etme umudu
Tıpta, genetik makas kanser için yeni immünoterapilere (: bağışıklık tedavilerine) katkıda bulunuyor ve kalıtsal hastalıkları tedavi etme düşünü gerçeğe dönüştürmek için deneyler yapılıyor. Halen araştırmacılar, orak hücre anemisi, beta talasemi gibi kan hastalıklarını ve kalıtsal göz hastalıklarını tedavi etmekte CRISPR / Cas9 kullanıp kullanamayacaklarını araştırmak amacıyla klinik denemeleri sürdürüyorlar.
Ayrıca beyin ve kaslar gibi büyük organlardaki genleri onarmak için yöntemler geliştiriyorlar. Hayvan deneyleri, özel olarak tasarlanmış virüslerin, istenen hücreler için genetik makasları verebileceğini gösteriyor. Böylece, kas distrofisi, spinal müsküler atropi ve Huntington hastalığı gibi omurga gibi yıkıcı kalıtsal hastalık tiplerinin tedavisinin mümkün olacağı görülüyor. Ancak, insan testlerine başlamadan önce, teknolojinin daha iyi hale getirilmesi gerekiyor.
Genetik makasın gücü düzenleme gerektirir
Genetik makas tüm faydalarının yanı sıra kötüye de kullanılabilir. Örneğin, bu araç genetiği değiştirilmiş embriyolar oluşturmak için. Kullanılabilir. Bununla birlikte, genetik mühendisliğinin uygulanmasını kontrol eden ve değiştirmeye yönelik yasakları içeren yasalar ve düzenlemeler uzun yıllardan beri yürürlüktedir. Bu düzenlemeler, insan genomunda, bir sonraki nesle geçebilecek kalıtsal değişiklikler yapılmasını yasaklamaktalar. Ayrıca, içeren deneyler insanların ve hayvanların dahil edildiği deneylerin yürütülmeye başlanmadan önce etik kurullar tarafından incelenip onaylanması zorunludur.
Kesin olan şu ki, bu genetik makaslar hepimizi etkiliyor. Yeni etik sorunlarla da karşılaşacağız, ancak bu yeni araç şu anda insanlığın karşı karşıya olduğu zorlukların çoğunun çözülmesine katkıda bulunabilir. Emmanuelle Charpentier ve Jennifer Doudna, yaşam bilimlerini yeni bir çağa taşıyan kimyasal bir araç geliştirdiler. Hayal edilemen potansiyele sahip geniş ufuklara bakmamızı sağladılar. Bu yeni alanda ilerledikçe, yeni ve beklenmedik buluşlar yapacağımız da kesin görünüyor.
İLERİ OKUMA
Bilimsel Açıklama metninin İngilizcesi de dahil olmak üzere bu yılki ödüllerle ilgili basın konferanslarının video görüntülerine, Nobel Konferanslarına ve daha fazla ek bilgiye İsveç Kraliyet Bilimler Akademisi'nin www.kva.se web sitesinden ve www.nobelprize.org adresinden ulaşabilirsiniz.
Derleyen: Mustafa Tunçgenç